Exemplos de potenciais efeitos secundários/eventos adversos incluem:
- Cefaleias
- Náuseas (sensação de enjoo)
- vómitos
Um evento adverso (EA), também conhecido como efeito secundário, é uma resposta indesejada e não intencional num doente, após a administração de um medicamento, que pode ou não ter sido causada pelo tratamento com este produto. Incluem-se aqui todos os eventos em que a utilização de um dispositivo médico cause lesões ou uma resposta não intencional e indesejada num paciente, utilizador ou outra pessoa. As informações que fornecer ajudam a garantir a segurança dos nossos produtos e pacientes.
Relativamente a Columvi (Glofitamab), Enspryng (satralizumab), Evrysdi (risdiplam), Lunsumio (mosunetuzumab), Piasky (crovalimab), Ronapreve (casirivimab & imdevimab), Rozlytrek (entrectinib), Vabysmo (faricimab), Itovebi (inavolisib):
▼ Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais de saúde que notifiquem quaisquer suspeitas de reações adversas. Se tiver quaisquer efeitos secundários fale com o seu médico ou enfermeiro.
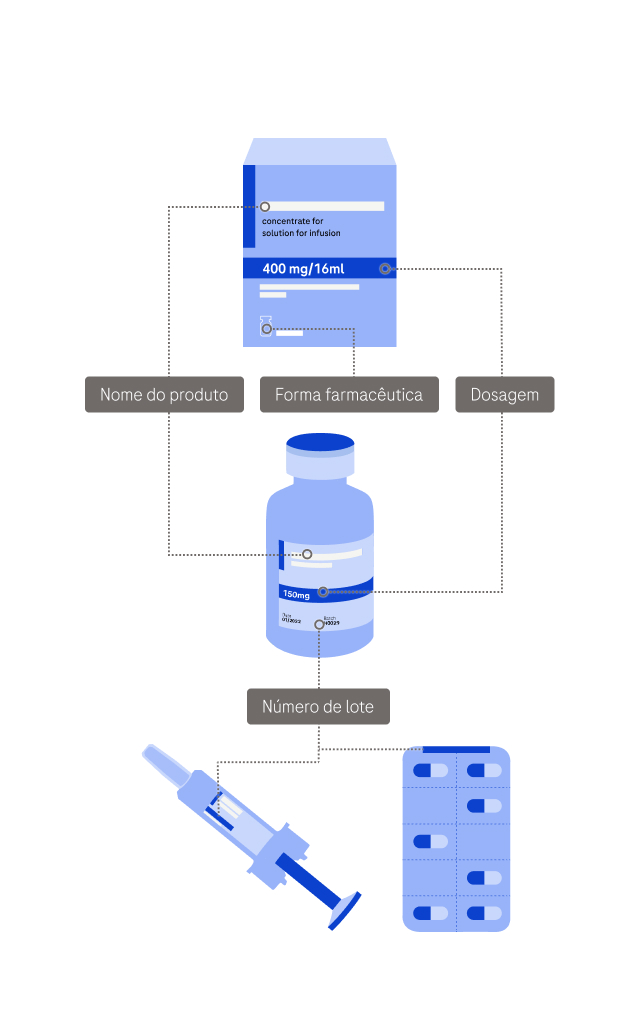
Os efeitos secundários podem incluir (mas não se limitam a) sintomas como:
Descreva o evento adverso da forma mais pormenorizada possível, como por exemplo: - O [efeito secundário] ocorreu depois de usar [o nome do produto] no [data]. O [efeito secundário] iniciou-se a [data] e o doente foi hospitalizado. O [efeito secundário] resolveu-se a [data].
As perguntas relacionadas com a gravidez têm como objetivo recolher informação sobre efeitos secundários e gravidez. Obrigado por contribuir para que os nossos produtos sejam mais seguros e mais eficientes.
Descreva aqui o efeito secundário, se já foi resolvido ou se ainda persiste, qual a sua gravidade, o resultado e quaisquer outras informações que possam ser relevantes antes, durante e após a ocorrência do efeito secundário. Para dispositivos médicos, descreva também a forma como o dispositivo causou ou contribuiu para o evento e, se relevante, descreva claramente a avaria do dispositivo que causou o evento.
A informação sobre a utilização dos nossos medicamentos durante a gravidez é importante para aumentar o conhecimento sobre a sua segurança e informar as doentes. Tenha em consideração que as doentes devem consultar o seu profissional de saúde para serem informadas sobre a segurança de tomar um medicamento durante a gravidez.
Todos os detalhes (pelo menos um detalhe identificador) que possa fornecer são importantes para melhorar a segurança dos nossos medicamentos. Os dados serão guardados em conformidade com os regulamentos de proteção de dados.
Se autoriza contactar o profissional de saúde que o assiste, indique os dados baixo
Informamos que para efeitos de cumprimento de obrigações legais, a Roche Farmacêutica Química, Lda. irá recolher e notificar às Autoridades de Saúde, quaisquer potenciais eventos adversos de que tome conhecimento. Os dados pessoais partilhados serão tratados de forma confidencial e de acordo com a legislação aplicável às atividades de farmacovigilância, conforme descrito na Política de Privacidade para a Farmacovigilância, Informação Médica e Reclamações de Qualidade, sendo os mesmos mantidos numa base de dados de farmacovigilância, para referência e cumprimento de obrigações legais e regulamentares, e eliminados findo o prazo legalmente estabelecido.
A Roche não poderá receber ou ter acesso a qualquer informação ou documentação que permita, de forma direta, a identificação de doentes. Assim, e de forma a dar cumprimento às obrigações legais a que V. Exa. e a Roche se encontram adstritas, solicitamos que antes de disponibilizar qualquer dado pessoal de terceiros à Roche, se certifique que não se encontra impedido de o fazer e que dispõe de consentimento expresso ou autorização legal (ou outra base de licitude de suporte ao tratamento) e que o titular dos dados tem conhecimento da comunicação dos seus dados à Roche.
Consulte informação detalhada sobre os tratamentos de dados pessoais levados a cabo na Roche na nossa Política de Privacidade.
By following this link, you are leaving Medical Information and entering a website that is not owned or controlled by Roche. Roche does not take any responsibility for access to or use of this website, nor for any content therein.